Hỗn dịch uống Trileptal 60mg/ml điều trị động kinh (chai 100ml)
P16300
Thương hiệu: NovartisDanh mục
Hoạt chất
Chỉ định
Dạng bào chế
Nơi sản xuất
Quy cách
Lưu ý
Đặt thuốc theo toa
Tải lên đơn thuốc của bạn để nhận sự tư vấn và hỗ trợ từ các dược sĩ của chúng tôi.

Mô tả sản phẩm
Thành phần
Thành phần hoạt chất: 1ml hỗn dịch uống chứa 60mg oxcarbazepine
Thành phần tá dược: Propyl parahydroxybenzoate (E 216); natri saccharin; acid sorbic (E 200); macrogot stearate 400; methyl parahydroxybenzoate (E 218); chất tạo hương vị chanh-mận màu vàng; acid ascorbic (E300); cellulose phân tán; propylen glycol; sorbitol 70% (không kết tinh); nước tinh khiết.
Ethanol là một thành phần của chất tạo hương vị.
Chỉ định (Thuốc dùng cho bệnh gì?)
Trileptal được chỉ định để điều trị các cơn động kinh cục bộ có hoặc không có các cơn động kinh co cứng - giật rung phát triển toàn thể thứ phát
Chống chỉ định (Khi nào không nên dùng thuốc này?)
Đã biết quá mẫn với oxcarbazepine hoặc eslicarbazepine hoặc bất kỳ tá dược nào của Trileptal.
Liều dùng
Trong đơn trị liệu và điều trị phối hợp, điều trị với Trileptal được khởi đầu bằng một liều có hiệu quả lâm sàng chia làm 2 lần. Có thể tăng liều tùy thuộc vào đáp ứng lâm sàng của bệnh nhân. Khi thay thế các thuốc chống động kinh khác bằng Trileptal nên giảm dần dần liều thuốc chống động kinh dùng đồng thời lúc bắt đầu điều trị bằng Trileptal. Trong điều trị phối hợp, vì tổng lượng thuốc chống động kinh trên bệnh nhân tăng nên có thể cần phải giảm liều các thuốc chống động kinh dùng đồng thời và/hoặc tăng liều Trileptal chậm hơn ( xem phần TƯƠNG TÁC, TƯƠNG KỴ CỦA THUỐC ). Nên kê đơn hỗn dịch uống Trileptal theo mililit (xem bảng chuyển đổi dưới đây tử liều miligam thành mililit). Liều được kê đơn bằng mililit được làm tròn đến 0,5ml gần nhất. Các liều được nêu trong bảng dưới đây chỉ có thể áp dụng cho bệnh nhân 6 tuổi trở lên . Những liều này được sử dụng 2 lần/ngày.
Bảng 1- Liều dùng tính theo miligam và mililit
Liều tính bằng miligam (dùng 2 lần/ngày) | Liều tính bằng mililit (dùng 2 lần/ngày) |
45 - 75mg | 1.0ml |
76-105mg | 1,5ml |
106-135mg | 2,0ml |
136-165mg | 2,5ml |
166-195mg | 3,0ml |
196-225mg | 3,5ml |
226-255mg | 4,0ml |
256-285mg | 4,5ml |
286-315mg | 5,0ml |
316-345mg | 5,5ml |
346-375mg | 6,0ml |
376-405mg | 6,5ml |
406-435mg | 7,0ml |
436-465mg | 7,5ml |
466-495mg | 8,0ml |
496-525mg | 8,5ml |
526-555mg | 9,0ml |
556-585mg | 9,5ml |
586-615mg | 10,0ml |
616-645mg | 10,5ml |
646-675mg | 11,0ml |
676-705mg | 11,5ml |
706-735mg | 12,0ml |
736-765mg | 12Ì5ml |
766-795mg | 13,0ml |
796-825mg | 13,5ml |
826-855mg | 14,0ml |
856-885mg | 14,5ml |
886-915mg | 15,0ml |
916-945mg | 15,5ml |
946-975mg | 16,0ml |
976-1.005mg | 16,5ml |
1.006-1.035mg | 17,0ml |
1.036-1.065mg | 17,5ml |
1.066-1.095 mg | 18.0ml |
1.096-1.125mg | 18,5ml |
1.126-1.155mg | 19.0ml |
1.156-1.185mg | 19,5ml |
1 186-1.215mg | 20,0ml |
Theo dõi và điều trị
Hiệu quả điều trị của oxcarbazepine chủ yếu thông qua chất chuyển hóa hoạt động là dẫn chất 10 - monohydroxy ( HD ) của Oxcartazapine ( xem phần ĐẶC TÍNH DƯỢC LỰC HỌC ).
Việc theo dõi nồng độ trong huyết tương của oxcarbazepine hoặc MHD không được đảm bảo thường quy. Tuy nhiên , có thể có ích trong trường hợp nghi ngờ có sự thay đổi độ thanh thải MHD ( xem phần CẢNH BÁO VÀ THẬN TRỌNG ).
Trong những trường hợp trên, liều Trileptal có thể phải được điều chỉnh ( dựa vào nồng độ thuốc trong huyết tương ,đo được sau 2-4 giờ sau liều uống ) để duy trì nồng độ đỉnh trong huyết tương của MHD <35mg/l
Người lớn
Đơn trị liệu
Liều khởi đầu khuyến cáo
Nên bắt đầu Trileptal với liều 600mg/ngày (8-10mg/kg/ngày) chia làm 2 lần.
Liều duy trì
Nếu được chỉ định trên lâm sàng, có thể tăng liều thêm một lượng tăng tối đa là 600 mg/ngày cách khoảng chừng mỗi tuần từ liều khởi đầu cho đến khi đạt được đáp ứng lâm sàng mong muốn. Đã ghi nhận hiệu quả điều trị ở các liều từ 600 mg/ngày đến 2.400mg/ngày.
Các thử nghiệm đơn trị liệu có đối chứng ở bệnh nhân không phải đang được điều trị bằng thuốc chống động kinh đã cho thấy liều có hiệu quả là 1,200 mg/ngày, tuy nhiên, liều 2.400mg/ngày đã được chứng minh có hiệu quả ở bệnh nhân kháng trị hơn được chuyển từ đơn trị liệu bằng các thuốc chống động kinh khác sang đơn trị liệu bằng Trileptal.
Liều tối đa khuyến cáo
Trong điều kiện được kiểm soát tốt tại bệnh viện, liều dùng tăng đến 2.400 mg/ngày đã đạt được sau 48 giờ.
Điều trị phối hợp
Liều khởi đầu khuyến cáo
Nên bắt đầu Trileptal với liều 600mg/ngày (8-10mg/kg/ngày) chia làm 2 lần.
Liều duy trì
Nếu được chỉ định trên lâm sàng, có thể tăng liều thêm một lượng tăng tối đa là 600 mg/ngày cách khoảng chừng mỗi tuần từ liều khởi đầu cho đến khi đạt được đáp ứng lâm sàng mong muốn. Đã ghi nhận hiệu quả điều trị ở các liều từ 600 mg/ngày đến 2.400 mg/ngày
Liều tối đa khuyến cáo
Trong một thử nghiệm điều trị phối hợp có đối chứng, các liều hàng ngày từ 600-2.400 mg/ngày đã được chứng minh là có hiệu quả, mặc dù hầu hết bệnh nhân đã không thể dung nạp được liều 2.400mg/ngày nếu không giảm liều thuốc chống động kinh dùng đồng thời, chủ yếu là do các biến cố bất lợi liên quan đến hệ thần kinh trung ương (CNS). Liều hàng ngày trên 2.400mg/ngày chưa được nghiên cứu có hệ thống trong các thử nghiệm lâm sàng.
Người cao tuổi (từ 65 tuổi trở lên)
Không cần khuyến cáo liều đặc biệt cho bệnh nhân cao tuổi vì liều điều trị được điều chỉnh theo từng cá thể. Khuyến cáo điều chỉnh liều ở bệnh nhân cao tuổi có suy giảm chức năng thận độ thanh thải creatinine <30ml/phút) (xem thông tin bên dưới về liều cho bệnh nhân suy thận).
Khuyến cáo theo dõi chặt nồng độ natri máu ở bệnh nhân có nguy cơ hạ natri máu (xem phần CẢNH BÁO VÀ THẬN TRỌNG).
Bệnh nhân suy gan
Không cần điều chỉnh liều đối với bệnh nhân suy gan nhẹ đến trung bình. Trileptal chưa được nghiên cứu trên bệnh nhân suy gan nặng, vì vậy cần thận trọng khi dùng thuốc cho bệnh nhân suy gan nặng (xem phần ĐẶC TÍNH DƯỢC ĐỘNG HỌC).
Bệnh nhận suy thận
ở bệnh nhân suy chức năng thận (độ thanh thải creatinine dưới 30 ml/phút), nên bắt đầu trị liệu Trileptal với liều bằng một nửa liều khởi đầu thường dùng (300mg/ngày) và tăng liều theo những khoảng cách ít nhất là từng tuần để đạt được đáp ứng lâm sàng mong muốn (xem phần ĐẶC TÍNH DƯỢC ĐỘNG HỌC).
Việc tăng liều ở bệnh nhân suy thận có thể đòi hỏi phải theo dõi cẩn thận hơn.
Trẻ em
Liều khởi đầu khuyến cáo
Trong đơn trị liệu và điều trị phối hợp,
Trileptal nên được khởi đầu với liều 8-10mg/kg/ngày chia làm hai lần.
Liều duy trì
Trong các thử nghiệm điều trị phối hợp, liều duy trì là 30-46 mg/kg/ngày, đạt được sau 2 tuần, được thấy là có hiệu quả và dung nạp tốt ở trẻ em. Tác dụng điều trị được ghi nhận ở liều duy trì trung vị khoảng 30mg/kg/ngày.
Liều tối đa khuyến cáo
Nếu được chỉ định trên lâm sàng, có thể tăng liều thêm một lượng tối đa mỗi 10 mg/kg/ngày với khoảng cách giữa các lần là xấp xỉ 1 tuần kể từ liều khởi đầu, cho tới mức liều tối đa là 46 mg/kg/ngày, để đạt được đáp ứng lâm sàng mong muốn (xem mục ĐẶC TÍNH DƯỢC ĐỘNG HỌC).
Trileptal được khuyến cáo sử dụng cho trẻ em từ 6 tuổi trở lên. Tính an toàn và hiệu quả đã được đánh giá trong các thử nghiệm lâm sàng có đối chứng bao gồm khoảng 230 trẻ em dưới 6 tuổi (xuống đến 1 tháng tuổi).
Không khuyến cáo sử dụng Trileptal cho trẻ em dưới 6 tuổi vì tính an toàn và hiệu quả chưa được chứng minh đầy đủ.
Tất cả các khuyến cáo liều dùng ở trên (người lớn, người cao tuổi và trẻ em) đều dựa vào các liều đã nghiên cứu trong những thử nghiệm lâm sàng đối với tất cả các nhóm tuổi. Tuy nhiên, có thể xem xét các liều khởi đầu thấp hơn khi thích hợp.
Cách dùng
Trước khi sử dụng hỗn dịch uốngTrileptal, nên lắc mạnh chai thuốc ít nhất 10 giây và chuẩn bị liều ngay sau đó. Lượng hỗn dịch uống được kê nên được hút khỏi chai bằng ống uống đi kèm. Hỗn dịch uống Trileptal có thể được nuốt trực tiếp từ ống uống hoặc có thể được trộn với một cốc thủy tinh nước nhỏ trước khi sử dụng. Sau mỗi lần dùng, nên đóng chai và lau bên ngoài ống uống bằng một khăn giấy khô, sạch.
Trileptal có thể được dùng cùng hoặc không cùng với thức ăn.
Hướng dẫn sử dụng, xử lý và hủy bỏ
Trước khi dùng hỗn dịch uống Trileptal, nên lắc kỹ chai thuốc và chuẩn bị liều dùng ngay sau đó. Nên sử dụng ống bơm thuốc uống được cung cấp để rút lượng hỗn dịch uống đã được kê đơn từ chai thuốc. Lượng sử dụng nên được làm tròn tới 0,5 ml gần nhất khi sử dụng ống bơm 10 ml (được cung cấp cùng với chai 250ml cho trẻ lớn hơn và người lớn) và tới 0,1ml khi sử dụng ống bơm 1ml (được cung cấp cùng với chai chứa 100 ml cho trẻ nhỏ hơn). Có thể uống trực tiếp hổn dịch uống Trileptal từ ống bơm thuốc uống hoặc có thể pha trong một ly nước nhỏ ngay trước khi dùng. Sau mỗi lần dùng, đậy nắp chai lại và lau bên ngoài ống bơm thuốc uống bằng một khăn giấy khô sạch.
Đọc kỹ hướng dẫn dưới đây để bạn biết cách sử dụng thuốc này
Thông tin về bộ thuốc Có 3 bộ phận của bộ thuốc: | |
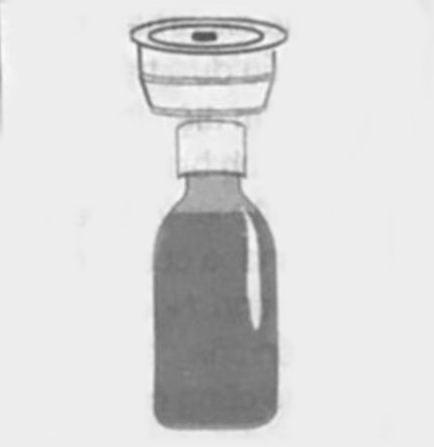 | 1.Bộ phận tiếp hợp bằng nhựa mà bạn ấn xuống cổ chai. Phải luôn giữ bộ phận này trong chai 2.Một chai chứa thuốc, có một nắp chống trẻ em. luôn đậy nắp sau khi dùng |
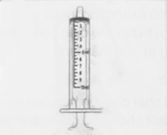 | 3.Một ống định liều uống. Ống này vừa với bộ phận tiếp hợp bằng nhựa để rút liều thuốc được kê đơn từ chai. |
| Cách chuẩn bị chai thuốc | |
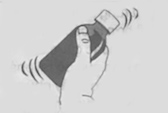 | 1. Lắc chai thuốc ít nhất 10 giây. 2. Tháo nắp chống trẻ em bằng cách ấn mạnh xuống và xoay nắp ngược chiều kim đồng hồ( như cho thấy trên đầu nắp). Lưu ý: Giữ nắp an toàn để đậy vào chai sau mỗi lần dùng |
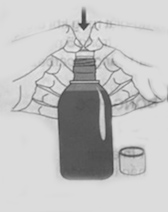 | 3. Giữ chai thuốc đã mở nắp thẳng đứng trên bàn. Ấn mạnh bộ phận tiếp hợp bằng nhựa vào cổ chai sâu với hết sức của bạn. 4. Đóng nắp tiếp hợp bằng nhựa vào cổ chai với hết sức của bạn Lưu ý:Bạn không thể ấn bộ phận tiếp hợp xuống hoàn toàn nhưng nó sẽ được đẩy mạnh vào chai khi bạn vặn nắp ngược lại. 5. Bây giờ chai thuốc đã sẵn sàng. Bộ phận tiếp hợp luôn gắn với chai thuốc. Để pha một liều, xin theo tất cả các hướng dẫn về Chuẩn bị một liều thuốc. |
| Chuẩn bị một liều thuốc | |
 | Có thể uống thuốc trực tiếp từ ống uống, hoặc pha một ly nước nhỏ. 1. Lắc kỹ chai thuốc. Chuẩn bị liều dùng ngay sau đó. 2. Ấn và xoay nắp chống trẻ em để mở chai (Lưu ý: Luôn đậy nắp lại sau khi dùng) |
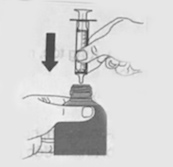 | 3. Kiểm tra piston để chắc chắn đã xuống hoàn toàn bên trong thân của ống uống. 4. Giữ chai thuốc thẳng đứng và đưa mạnh ống uống vào trong bộ phận tiếp hợp bằng nhựa. |
 | 5. Giữ ống uống ở tại chỗ và cẩn thận xoay ngược chai thuốc xuống dưới. 6. Kéo từ từ piston xuống dưới hoàn toàn để cho piston đầy thuốc. Đẩy piston ngược trở lên hoàn toàn để đẩy bất kỳ bọt khí lớn nào có thể còn kẹt bên trong ống uống. |
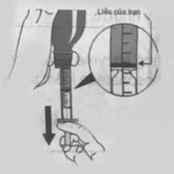 | 7. Rút liều được kê đơn: Kéo từ từ piston xuống cho đến khi gờ trên của vòng màu đen ở chính xác ngang mức có đánh dấu trên thân của ống uống chỉ ra liều được kê đơn. Lưu ý:Nếu liều được kê đơn nhiều hơn thể tích của ống uống nạp lại ống uống lên mức cần thiết để lấy lượng còn lại. |
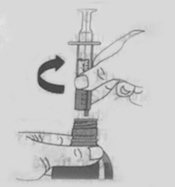 | 8. Cẩn thận xoay chai thuốc trở lại thẳng đứng . Rút ống uống ra bằng cách vặn nhẹ ống khỏi bộ phận tiếp hợp bằng nhựa. Bộ phận tiếp hợp nên nằm bên trong chai. |
 | 9. Liều thuốc này có thể uống trực tiếp từ ống uống. Bệnh nhân phải ngồi ở tư thế thẳng đứng và phải đẩy piston từ từ để cho bệnh nhân nuốt. Một cách khác là có thể pha liều này trong một ly nước nhỏ ngay trước khi dùng. Khuấy và uống toàn bộ hỗn dịch này ngay. 10. Đậy nắp chống trẻ em lại sau khi dùng, để bộ phận tiếp hợp ở lại tại chỗ. 11. Lau sạch: Sau khi dùng, lau bên ngoài ống uống bằng một khăn giấy khô, sạch. |
Tác dụng phụ
Tác dụng không mong muốn (Tác dụng phụ)
Tóm tắt dữ liệu an toàn
Các phản ứng phụ đã được báo cáo thường gặp nhất là buồn ngủ, nhức đầu, chóng mặt, song thị, buồn nôn, nôn và mệt mỏi xảy ra ở hơn 10% bệnh nhân.
Trong các thử nghiệm lâm sàng, các biến cố bất lợi (AE) thường ở mức độ từ nhẹ trung bình, có tính chất thoáng qua và hay gặp hơn khi khởi đầu điều trị
Phân tích biểu đồ tác dụng không mong muốn theo hệ cơ quan của cơ thể dựa trên những biến cố bất lợi từ những thử nghiệm lâm sàng đã được đánh giá là liên quan với Trileptal. Ngoài ra. các báo cáo có ý nghĩa lâm sàng về phản ứng phụ từ các (chương trình với bệnh nhân được xác định và kinh nghiệm hậu mãi cũng đà được tính đến.
Bảng tóm tắt tổng hợp các phản ứng bất lợi từ các thử nghiệm lâm sàng
Các phản ứng bất lợi từ các thử nghiệm lâm sàng (Bảng 3) được liệt kê theo hệ thống phân loại cơ quan MedDRA. Trong mỗi hệ thống cơ quan, phản ứng bất lợi được xếp thứ tự theo tần suất với phản ứng có tần suất cao nhất đứng trước. Trong mỗi nhóm tần suất, phản ứng bất lợi được xếp theo thứ tự giảm dần mức độ nghiêm trọng. Thêm vào đó, nhóm tần suất tương g ứng được xếp theo qui ước sau (CIOMS III): Rất thường gặp ( ≥1/10); thường gặp: (≥1/100 đến<1/10); ít gặp. (≥1/1 000 đến <1/100); hiếm gặp: (≥1/10.000 đến <1/1.000); rất hiếm gặp: (<1/10.000).
Bảng 3: Các phản ứng bất lợi của thuốc
| Rối loạn máu và hệ bạch huyết | |
| Ít gặp | Giảm bạch cầu. |
| Rất hiếm gặp | Suy tủy xương, thiếu máu bất sản, mất bạch cầu hạt, giảm toàn thể huyết cầu, giảm tiểu cầu, giảm bạch cầu trung tính. |
| Rối loạn hệ miễn dịch | |
| Rất hiếm gặp | Phản ứng phản vệ, quá mẫn cảm (bao gồm quá mẫn cảm nhiều cơ quan) được đặc trưng bởi các biểu hiện như nổi ban, sốt. Các cơ quan hoặc hệ thống khác có thể bị ảnh hưởng như máu và hệ bạch huyết (ví dụ tăng bạch cầu ưa eosin, giảm tiểu cầu, giảm bạch cầu, bệnh hạch bạch huyết, lách to), gan (ví dụ: viêm gan, các xét nghiệm bất thường về chức năng gan), cơ và khớp (ví dụ: sưng khớp, đau cơ, đau khớp), hệ thần kinh (ví dụ: bệnh não gan), thận (ví dụ: suy thận, viêm thận kẽ, protein niệu), phổi (ví dụ: phù phổi, hen, co thắc phế quản, bệnh phổi kẽ, khó thở), Phù mạch |
Rối loạn nội tiết | |
| Thường gặp | Tăng cân |
| Rất hiếm gặp | Suy giáp |
RốI loạn chuyển hóa và dinh dưỡng | |
Thường gặp | Giảm natri huyết |
| Rất hiếm gặp | Giảm natri huyết* liên quan với các dấu hiệu và triệu chứng như co giật, bệnh não, giảm ý thức, lú lẫn (xem thêm Rối loạn hệ thần kinh để rõ thêm các phản ứng bất lợi), suy giáp rối loạn thị giác (ví dụ nhìn mờ), suy giáp, nôn, buồn nôn, thiếu hụt acid folic. |
Rối loạn tâm thần | |
| Thường gặp | Kích động (ví dụ: căng thẳng thần kinh), cảm xúc không ổn định, tình trạng lú lẫn, trầm cảm, vô cảm. |
Rối loạn hệ thần kinh | |
Rất thường gặp | Buồn ngủ, nhức đầu, chóng mặt. |
| Thường gặp | Mất điều hòa, run, rung giật nhãn cầu, rối loạn sự chú ý, mất trí nhớ. |
Rối loạn mắt | |
| Rất thường gặp | Song thị. |
| Thường gặp | |
| Nhìn mờ, rối loạn thị giác. | |
Rối loạn tai và mê đạo | |
| Thường gặp | Chóng mặt. |
Rối loạn tim | |
| Rất hiếm gặp | Block nhĩ thất, loạn nhịp. |
Rối loạn mạch | |
| Không rõ | Tăng huyết áp. |
Rối loạn tiêu hóa | |
| Rất thường gặp | Nôn, buồn nôn. |
| Thường gặp | Tiêu chảy, đau bụng, táo bón. |
Rất hiếm gặp | Viêm tụy và/hoặc tăng lipase và/hoặc tăng amylase |
Rối loạn gan mật | |
| Rất hiếm gặp | Viêm gan |
| Rối loạn da và mô dưới da | |
Thường gặp | Phát ban, rụng tóc, mụn trứng cá. |
| Ít gặp | Nổi mề đay |
| Rất hiếm gặp | Hội chứng Stevens-Johnson, hoại tử biểu bì nhiễm độc (hội chứng Lyell), phù mạch, ban đỏ đa hình. |
| Rối loạn cơ xương, mô liên kết và xương | |
| Rất hiếm gặp | |
| Lupus ban đỏ hệ móng. | |
| Rối loạn toàn thân và tình trạng tại chỗ dùng thuốc | |
| Rất thường gặp | Mệt mỏi. |
| Thường gặp | Suy nhược. |
| Xét nghiệm | |
| Ít gặp | Tăng enzyme gan, tăng phosphatase kiềm trong máu. |
| Không rõ | Tăng amylase, tănglipase. |
*Giảm natri huyết có ý nghĩa lâm sàng rất hiếm gặp (natri <125 mmol/l) có thể phát sinh trong khi dùng Trileptal. Trường hợp này thường xảy ra trong 3 tháng đầu điều trị bằng Trileptal, mặc dù có những bệnh nhân có natri huyết thanh < 125 mmol/1 lần đầu tiên hơn 1 năm sau khi khởi đầu điều trị (xem phần CẢNH BÁO VÀ THẬN TRỌNG).
Các phản ứng phụ của thuốc từ các báo cáo tự phát và các trường hợp trong y văn (không rõ tần suất)
Các phản ứng phụ của thuốc sau đây có nguồn gốc từ kinh nghiệm hậu mãi với Trileptal thông qua các báo cáo tự phát và các trường hợp trong y văn. Vì những phản ứng này đã được báo cáo tự nguyện từ một nhóm dân số có quy mô không xác định, không thể ước tính đáng tin cậy về tần suất, vì vậy được phân loại là không rõ. Những tác dụng không muốn được liệt kê dưới đây theo phân loại hệ cơ quan của MedDRA. Trong mỗi hệ cơ quan, ADRs được ghi nhận theo trình tự giảm dần về độ nghiêm trọng.
Rối loạn chuyến hóa và dinh dưỡng
Hội chứng tiết ADH không thích hợp, với dấu hiệu và triệu chứng như thờ ơ, buồn nôn, chóng mặt, giảm thẩm thấu huyết thanh (máu), nôn, nhức đầu, lú lẫn hoặc các dấu hiệu và triệu chứng thần kinh khác.
Rối loạn da và mô dưới da
Phát ban do thuốc với tăng bạch cầu eosin và các triệu chứng hệ thống (DRESS), ngoại ban mụn mủ toàn thân cấp tính (AGEP).
Chấn thương ngộ độc và các biến chứng phẩu thuật
Té ngã
Rối loạn hệ thần kinh
Rối loạn ngôn ngữ (bao gồm loạn vận ngôn), thường gặp nên khi tăng liều Trileptal
Rối loạn cơ xương, mô liên kết và xương
Đã có báo cáo về giảm mật độ xương, giảm xương, loãng xương và gãy xương ở bệnh nhân đang điều trị dài hạn bằngTrileptal. Cơ chế oxcarbazepine ảnh hưởng đến sự chuyển hóa của xương chưa được xác định.
Thận trọng (Những lưu ý khi dùng thuốc)
Quá mẫn
Phản ứng quá mẫn loại I (xảy ra tức thì) bao gồm nổi ban, ngứa, nổi mề day, phù mạch và các báo cáo về phản vệ đã nhận được trong giai đoạn hậu mãi. Đã có báo cáo về các trường hợp phản vệ và phù mạch bao gồm cả thanh quản, thanh môn, môi và mí mắt ở bệnh nhân sau khi uống các liều Trileptal đầu tiên hoặc các liều kế tiếp.
Nếu bệnh nhân gặp các phản ứng này sau khi điều trị bằng Trileptal, phải ngưng dùng thuốc và bắt đầu điều trị bằng một thuốc thay thế.
Nên báo cho những bệnh nhân đã từng bị phản ứng quá mản với carbamazepine là khoảng 25-30% số bệnh nhân này có thể có phản ứng quá mẫn với Trileptal (xem phần PHẢN ỨNG BẤT LỢI).
Phản ứng quá mẫn, bao gồm phản ứng quá mẫn ở nhiều cơ quan cũng có thể xảy ra ở bệnh nhân không có tiền sử quá mẫn với carbamazepine. Những phản ứng này có thể ảnh hưởng đến da, gan, máu và hệ bạch huyết hoặc các cơ quan khác, xảy ra riêng lẻ hoặc kết hợp với nhau trong bệnh cảnh phản ứng toàn thân (xem phần PHẢN ỨNG BẤT LỢI). Nói chung, nó có các dấu hiệu và triệu chứng gợi ý phản ứng quá mẫn, phải ngừng dùng Trileptal ngay lập tức.
Tác dụng trên da
Các phản ứng ngoài da nghiêm trọng, bao gồm hội chứng Stevens-Johnson, hoại tử biểu bì nhiễm độc (hội chứng Lyell) và ban đỏ đa dạng đã được báo cáo là rất hiếm gặp liên quan với việc sử dụng Trileptal. Bệnh nhân bị các phản ứng da nghiêm trọng có thể cần phải nhập viện vì các tình trạng này có thể đe dọa tính mạng và trong trường hợp rất hiếm có thể gây tử vong. Các trường hợp liên quan đến Trileptal xảy ra ở cả trẻ em và người Iớn. Thời gian khởi phát trung bình là 19 ngày. Vài trường hợp riêng lẻ có tái phát phản ứng da nghiêm trọng khi dùng lại Trileptal đã được báo cáo Khi bệnh nhân gặp phản ứng ngoài da với Trileptal, cần cân nhắc ngừng dùng Trileptal và thây thế bằng thuốc chống động kinh khác.
Gen dược học
Ngày càng có nhiều bằng chứng cho thấy các gen đồng vị khác nhau (alen) của kháng nguyên tế bào bạch cầu ở người (HLA) đóng vai trò liên quan đến các phản ứng phụ trên da ở những bệnh nhân dễ mắc.
Liên quan đến HLA-BM502
Các nghiên cứu hồi cứu ở bệnh nhân người Hán gốc Trung Quốc và người Thái cho thấy tương quan mạnh giữa các phản ứng da SJS/TEN do carbamazepine và những bệnh nhân có kháng nguyên bạch cầu người HLA-B*1502. Bởi vì cấu trúc hóa học của oxcarbazepine tương tự với cấu trúc của carbamazepine, có khả năng cho rằng những bệnh nhân mang gen đồng vi HLA-B*1502 cũng gia tăng nguy cơ phản ứng da SJS/TEN với oxcarbazepine.
Tần số của gen đồng vị HLA-B*1502 là 2-12% dân số người Hán Trung Quốc, khoảng 8% người dân Thái, hơn 15% ở Philipines và một số người Malaysia. Tần số gen đồng vị này lên đến lần lượt là 2% ở Hàn Quốc và 6% ờ Ấn Độ. Tần số của HLA-B*1502 thì không đáng kể ở những người gốc Châu Âu, một vài chủng tộc ở Châu Phi, người Mỹ bản xứ, người gốc Tây Ban Nha và Nhật Bản ( < 1%).
Tần số gen đồng vị được liệt kê ở đây đại diện cho phần trăm nhiễm sắc thể ở những dân số đặc biệt mà có gen đồng vị này, nghĩa là phần trăm mà bệnh nhân mang bản sao của gen đồng vị này trên ít nhất 1 trong hai nhiễm sắc thể của chúng nâng số người mang*) là cao gần gấp đôi tần số của gen đồng vị. Vì vậy phần trăm bệnh nhân có nguy cơ thì gần gấp đôi tần số gen đồng vị.
Kiểm tra sự hiện diện của gen đồng vị HLA-B*1502 nên được xem xét ở các bệnh nhân có tổ tiên thuộc nhóm dân số nguy cơ về mặt di truyền, trước khi khởi đầu điều trị bằngTrileptal (xem thông tin dành cho chuyên gia y tế bên dưới). Trileptal nên được tránh dùng cho các bệnh nhân mà kết quả thử nghiệm cho thấy dương tính với HLA-B*1502 trừ khi lợi ích vượt trội nguy cơ HLA-B*1502 có thể là một yếu tố nguy cơ của sự phát triển SJS/TEN ở dân số Trung Quổc sử dụng các thuốc chống động kinh khác (AED) không quan đến SJS/TEN. Vì vậy cần xem xét tránh dùng các thuốc liên quan đến SJS/TEN ở những bệnh nhân dương tính HLA-BM502, khi liệu pháp điều trị thay thế khác dược chấp nhân. Việc tầm soát không được khuyến cáo thực hiện với những nhóm bệnh nhân có tần số HLA-B*1502 thấp hoặc những bệnh nhân đang sử dụng Trileptal. Bởi vì nguy cơ của SJS/TEN giới hạn trong vài tháng đầu điều trị bất kể tình trạng của HLA-B*1502.
Liên quan đến HLA-A*3101
Kháng nguyên bạch cầu người (HLA)-A*3101 có thể là một yếu tố nguy cơ cho các phản ứng phụ ở da như SJS, TEN. DRESS, AGEP và chứng phát ban dát sần.
Tần số của gen đồng vị HLA-A*3101 thây đổi đa dạng giữa các dân tộc và tần số của nó vào khoảng 2 đến 5% ở dân số Châu Âu và khoảng 10% ở người Nhật. Tần số của gen đồng vị này ước đoán ít hơn 5% ở đa số dân ở Úc. Châu Á. Châu Phi và Bác Mỹ với một vài ngoại lệ là từ 5-12%. Tần số hơn 15% được ước lượng ở một số nhóm dân tộc như Nam Mỹ (Argentina và Brazil), Bắc Mỹ (thổ dân Navajo, Sioux và Mexico Sonora Seri) và Nam An (Tamil Nadu) và giữa 10-15% ở các dân tộc bản địa trong cùng khu vực.
Tần số gen đồng vị đưọrc liệt kê ở đây đại diện cho phần trăm nhiễm sắc thể ở những dân số đặc biệt mà có gen đồng vị này, nghĩa là phần trăm mà bệnh nhân mang bản sao của gen đồng vị này trên ít nhất 1 trong hai nhiềm sắc thể của chúng (“tần số người mang') là cao gần gấp đôi tần số của gen đồng vị. Vì vậy phần trăm bệnh nhân có nguy cơ gần gấp đôi tần số gen đồng vị.
Có số liệu cho rằng HLA-A*3101 liên quan đến sự gia tăng nguy cơ phản ứng bất lợi trên da do carbamazepine bao gồm SJS, TEN, chứng phát ban bởi thuốc kết hợp với tăng bạch cầu ưa acid (DRESS) do dị ứng. hoặc chứng phát ban mụn mủ cấp tính ít nghiêm trọng (AGEP) và phát ban dát sần. Không đủ dữ liệu cũng cố cho khuyến cáo tiến hành thử nghiệm sự hiện diện của gen đồng vị HLA-A*3101 ờ bệnh nhân trước khi khởi đầu điều trị với oxcarbazepine kiểm tra di truyền không khuyến cáo tiến hành cho bệnh nhân đang dùng Triteptal, bởi vì nguy cơ của SJS. TEN, DRESS và phát ban dát sần giới hạn phạm vi trong vài tháng đầu điều trị, bát kế tình trạng của HLA-A*3101.
Giới hạn của tầm soát di truyền
Kết qủa của tầm soát di truyền không bao giờ thay thế cho cảnh giác lâm sàng thích hợp và quản lý bệnh nhân. Nhiều bệnh nhân Châu Á dương tính với HLA-B* 1502 và điều trị bằng trileptal không bị SJS/TEN và bệnh nhân âm tính với HLA-B*1502 bất kì chủng tộc nào vì có thể bị SJS/TEN tương tự với các bệnh nhân dương tính HLA-A*3101 và dùng Trileptal không bị SJS/TEN. DRESS AGEP hoặc phát ban dát sần và các bệnh nhân âm tính HLA.A*3101 bất kì chủng tộc nào vì có thể bị các phản ứng phụ nặng trên da. Vai trò của các yếu tố tiềm năng khác trong sự phát triển và bệnh suất từ các phản ứng phụ trên da này ví dụ như liều AED, sự tuân thủ, sử dụng đồng thời với các thuốc khác, các bệnh khác đi kèm và mức độ giám sát về da chưa được nghiên cứu.
Thông tin cho các chuyên gia y tế
Nếu kiểm tra sự hiện diện của gen đồng vị HLA-B*1502 được thực hiện 'kiểu gen HLA-B*1502' phân giải cao được khuyến cáo. Thử nghiệm dương tính nếu một trong hai đồng vị HLA-B*1502 được phát hiện và âm tính nếu không phát hiện thấy gen đồng vị nào. Tương tự nếu kiểm tra sự hiện diện của gen đồng vị HLA-B*3101 được thực hiện, ' kiểu gen HLA-B*3101' phân giải cao được khuyến cáo. Thử nghiệm dương tính nếu một trong hai đồng vị HLA-B*3101 được phát hiện và âm tính nếu không phát hiện thấy gen đồng vị nào.
Nguy cơ tăng nặng tình trạng bệnh động kinh
Nguy cơ tăng nặng bệnh được báo cáo khi dùng Trileptal. Nguy cơ này được xem là đặc biệt ở trẻ em, nhưng cũng có thể xảy ra ở người lớn. Trong trường hợp tăng nặng, nên ngừng sử dụng Trileptal.
Giảm natri huyết
Nồng độ natri trong huyết thanh dưới 125mmol/l, thường không có triệu chứng và không cần chỉnh liều điều trị đã được quan sát thấy ở 2,7% bệnh nhân điều trị bằng Trileptal. Kinh nghiệm từ các thử nghiệm lâm sàng cho thấy nồng độ nằm trong huyết thanh trở về bình thường khi giảm liều, ngừng dùng Trileptal hoặc bệnh nhân được điều trị bảo tồn (ví dụ hạn chế thu nhận dịch).
Với bệnh nhân đã có bệnh thận từ trước, kèm theo thiếu hụt hàm lượng natri (như hội chứng tiết ADH không phù hợp) hoặc với bệnh nhân dùng phối hợp thuốc thải natri (ví dụ: thuốc lợi niệu, thuốc làm bài tiết không thích đáng ADH), nên định lượng nồng độ natri huyết thanh trước khi bầt đầu điều trị. Sau đó, nên định lượng nồng độ natri huyết thanh sau khoảng 2 tuần rồi theo các khoảng cách từng tháng trong 3 tháng đầu điều trị hoặc theo yêu cầu của lâm sàng. Đặc biệt những yếu tố nguy cơ này có thể xảy đến cho bệnh nhân cao tuổi.
Đối với bệnh nhân đang điều trị bằng Trileptal mà bắt đầu dừng dùng thuốc làm giảm natri thì cần tiến hành kiểm tra natri theo cách như trên. Nói chung, nếu triệu chứng lâm sàng gợi ý có giảm natri huyết khi đang dùng Trileptal ( xem phần PHẢN ỨNG BẤT LỢI) thì có thể phải xem xét định lượng natri huyết thanh. Đối với những bệnh nhân khác, có thể đánh giá huyết thanh như một phần nghiên cứu thường quy trong phòng thí nghiệm.
Tất cả các bệnh nhân suy giảm chức năng tim và suy tim thứ phát cần được kiểm tra cân nặng thường xuyên để xác định sự ứ dịch. Trong trường hợp ứ dịch hoặc tình trạng tim xấu đi, cần kiểm tra natri huyết thanh. Nếu thấy giảm natri huyết thì biện pháp xử trí quan trọng là hạn chế dùng nước. Vì trong rất hiếm trường hợp oxcarbazepine có thể dẫn đến suy yếu dẫn truyền tim, cần theo dõi cẩn thận bệnh nhân bị rối loạn dẫn truyền có từ trước (ví dụ block nhĩ thất, loạn nhịp).
Suy giáp
Suy giáp là một phản ứng bất lợi rất hiếm của oxcarbazepine. Vì tầm quan trọng hormon tuyến giáp với sự phát triển của trẻ sau sinh, nên đánh giá chức năng tuyến giáp trước khi bắt đầu điều trị với Trileptal ở nhóm bệnh nhân trẻ em. Khuyến cáo theo dõi chức năng tuyến giáp khi điều trị với Trileptal ở nhóm bệnh nhân trẻ em.
Chức năng gan
Rất hiếm gặp viêm gan đã được báo cáo, hầu hết trường hợp đều được xử trí dễ dàng. Nếu nghi ngờ viêm gan, nên cân nhắc ngừng dùng Trileptal. Thận trọng khi điều trị với bệnh nhân suy gan nặng (xem phần LIỀU DÙNG VÀ CÁCH DÙNG và phần ĐẶC TíNH DƯỢC ĐỘNG HỌC).
Chức năng thận
Thận trọng khi dùng Trileptal cho bệnh nhân suy giảm chức năng thận (độ thanh thải creatinine nhỏ hơn 30ml/phút). Đặc biệt khi dùng liều khởi đàu và khi tăng liều (xem phần LIỀU DÙNG VÀ CÁCH DÙNG và phần ĐẶC TÍNH DƯỢC ĐỘNG HỌC).
Tác dụng về huyết học
Đã có báo cáo trong trường hợp rất hiếm về chứng mất bạch cầu hạt, thiếu máu bất sản và giảm toàn thể huyết cầu ở những bệnh nhân được điều trị bằng Trileptal theo kinh nghiệm hậu mãi (xem phần PHẢN ỨNG BẤT LỢI) Tuy nhiên, do tỷ lệ mắc mới các tình trạng này rất thấp và các yếu tố nhiễu (ví dụ như bệnh chính, thuốc dùng đồng thời), không thể xác định được quan hệ nhân quả.
Nên xem xét ngừng dùng thuốc nếu có bất kỳ dấu hiệu nào về suy tủy xương đáng kể.
Hành vi và ý định tự tử
Đã có báo cáo về ý nghĩ tự tử và hành vi tự tử ở bệnh nhân được điều trị bằng thuốc chống động kinh trong một số chỉ định. Một phân tích tổng hợp các thử nghiệm ngẫu nhiên có đối chứng với giả dược cũng cho thấy tăng nhẹ nguy cơ về ý nghĩ tự tử và hành vi tự tử. Chưa rõ cơ chế của nguy cơ này.
Vì vậy cần phải theo dõi bệnh nhân về các dấu hiệu của ý nghĩ tự tử và hành vi tự tự và nên xem xét điều trị thích hợp. Nên khuyên bệnh nhân ( và người chăm sóc bệnh nhân) tìm kiếm sự tư vấn y tế nếu xuất hiện ý nghĩ tự tử và hành vi tự tử.
Tương tác thuốc (Những lưu ý khi dùng chung thuốc với thực phẩm hoặc thuốc khác)
Thuốc tránh thai hormone
Phải cảnh báo cho bệnh nhân nữ trong tuổi sinh đẻ là việc dùng đồng thời Trileptal với thuốc tránh thai hormone có thể làm mất hiệu quả của loại thuốc tránh thai này (xem phần TƯƠNG TÁC, TƯƠNG KỴ CỦA THUỐC và phần PHỤ NỮ CÓ THAI, CHO CON BÚ VÀ KHẢ NĂNG SINH SẢN). Khuyến cáo sử dụng các dạng tránh thai khác không phải hormone khi đang dùng Trileptal.
Rượu
Nên thận trọng khi uống rượu kết hợp với việc điều trị bằng Trileptal do có thể tăng tác dụng làm buồn ngủ.
Tác dụng khi ngừng dùng thuốc
Cũng như với tất cả các thuốc chống động kinh khác, nên ngừng Trileptal từ từ để giảm thiểu khả năng tăng tuần suất cơn động kinh.
TƯƠNG TÁC, TƯƠNG KỴ CỦA THUỐC
Cảm ứng enzyme
In vitro và in vivo, oxcarbazepine và chất chuyển hóa có hoạt tính dược lý của nó (dẫn xuất monohydroxy, MHD) là những chất gây cảm ứng yếu các enzyme cytochrome P450 CYP3A4 và CYP3A5 chịu trách nhiệm đối với việc chuyển hóa một số rất lớn các loại thuốc, ví dụ thuốc ức chế miễn dịch (ví dụ ciclosporin, tacrolimus), thuốc tránh thai dạng uống (xem dưới đây) và một số thuốc chống động kinh khác (ví dụ carbamazepine) dẫn đến giảm nồng độ của những thuốc này trong huyết tương (xem bảng dưới đây tóm tắt kết quả của các thuốc chống động kinh khác).
In vitro, oxcarbazepine và MHD là những chất gây cảm ứng yếu UDP-glucuronyl transferase (chưa rõ tác dụng trên các enzyme đặc hiệu trong họ enzyme này). Vì vậy, in vivo oxcarbazepine và MHD có thể có tác dụng gây cảm ứng nhẹ trên sự chuyển hóa của các thuốc chủ yếu được thải trừ do sự liên hợp thông qua UDP- glucuronyl transferase. Khi bắt đầu điều trị. Bằng Trileptal hoặc khi thây đổi liều, có thể mất 2-3 tuần để đạt được cấp độ mới về cảm ứng.
Trong trường hợp ngừng điều trị bằng Trileptal, Có thể cần phải giảm liều các thuốc dùng dòng thời và nên quyết định dựa trên sự theo dõi trên lâm sàng và/hoặc nồng độ trong huyết tương. Sự cảm ứng có thể giảm dần dần sau 2-3 tuần sau khi ngừng điều trị.
Thuốc tránh thai hormone: Trileptal đã được biết là có ảnh hưởng trên hai thành phần là ethinylestradiol (EE) vồ levonorgestrel (LNG) của một thuốc tránh thai dạng uống. Các trị số diện tích dưới dường cong (AUC) trung bình của EE giảm 48-52% và của LNG giảm 32-52%. Vì vậy dùng đồng thời Trileptal với các thuốc tránh thai hormone có thể làm mất hiệu quá của các thuốc tránh thai này (xem phần CẢNH BÁO VÀ THẬN TRỌNG). Nên dùng một phương pháp tránh thai đáng tin cậy khác.
Ức chế enzyme
Oxcarbazepine và MHD ức chế CYP2C19. Vì vậy có thể xảy ra tương tác khi dùng kết hợp Trileptal liều cao với các thuốc chủ yếu được chuyển hóa bởi CYP2C19 (ví dụ phenytoin). Nồng độ phenytoin trong huyết tương tăng lên đến 40% khi Trileptal được dùng với các liều trên 1.200 mg ngày (xem bảng dưới đây tóm tắt kết quả với các thuốc chống động kinh khác). Trong trường hợp này có thể cần phải giảm liều phenytoin dùng kết hợp (xem phần LIỀU DÙNG VÀ CÁCH DÙNG).
Các thuốc chống động kinh khác và các thuốc gây cảm ứng enzyme.
Những tương tác tiềm năng giữa Trileptal và các thuốc chống động kinh khác đã được đánh giá qua các nghiên cứu lâm sàng. Ảnh hưởng của những tương tác này đến diện tích dưới đường cong(AUC) trung bình và nồng độ thấp nhất tronghuyeets tương (Cmin) được tóm tắt trong bảng 2 sau đây.
Bảng 2- Tóm tắt về tương tác của thuốc chống động kinh vơi Trileptal
Thuốc chống động kinh Dùng kết hợp | Ảnh hưởng của Trileptal đến thuốc chống động kinh Nồng độ | Ảnh hưởng của thuốc chống động kinh đến MHD Nồng độ |
Carbamazepine | Giảm 0-22% ( tăng 30% về Carbamazepine- epoxide) | Giảm 40% |
| Clobazam | Chưa được nghiên cứu | Không ảnh hưởng |
| Felbamate | Chưa được nghiên cứu | Không ảnh hưởng |
| Lamotrigine | Không ảnh hưởng | Không ảnh hưởng |
| Phenobarbitone | Tăng 14 - 15% | Giảm 30 - 31% |
| Phenytoin | Tăng 0 - 40% | Giảm 29 - 35% |
| Valproic acid | Không ảnh hưởng | Giảm 0 - 18% |
Những thuốc gây cảm ứng mạnh các enzyme cytochrome P450 và/hoặc UGT( tức là carbamazepine, phenytoin và phenobarbitone) đã cho thấy làm giảm nồng độ MHD trong huyết tương (29-49%) ở người lớn và trẻ em 4-12 tuổi, độ thanh thải MHD tăng khoảng 35% khi dùng một trong 3 thuốc chống động kinh gây cảm ứng enzyme so với đơn trị liệu. Điều trị đồng thời Trileptal và lamotrigine có liên quan với tăng nguy cơ các phản ứng phụ (buồn nôn, buồn ngủ, chóng mặt và nhức đầu). Khi dùng đồng thời một hoặc vài thuốc chống động kinh với Trileptal, có thể cần phải xem xét điều chỉnh liều cẩn thận và/hoặc theo dõi nồng độ trong huyết tương trên cơ sở từng trường hợp đặc biệt là ở bệnh nhi được điều trị đồng thời với lamotngine.
Chưa quan sát thấy sự tự cảm ứng với Trileptal.
Các tương tác thuốc khác
Cimetidine, erythromycin, viloxazine, warfarin và dextropropoxyphene không có tác dụng trên dược động học của MHD.
Tương tác giữa oxcarbazepine và thuốc ức chế monoamine oxidase (MAOI) về mặt lý thuyết có thể dựa trên mốii liên quan về cấu trúc của oxcarbazepine với thuốc chống trầm cảm ba vòng.
Những bệnh nhân đang điều trị bằng thuốc chống trầm cảm ba vòng đã được đưa vào các thử nghiệm lâm sàng và không quan sát thấy tương tác nào có ý nghĩa lâm sàng.
Sự kết hợp lithium và oxcarbazepine có thể làm tăng độc tính đối với thần kinh.
Tính tương kỵ
Do không có các nghiên cứu về tính tương kỵ của thuốc, không trộn lẫn thuốc này với các thuốc khác.
Bảo quản: Bảo quản dưới 30 độ C. Bảo quản thuốc trong bao bì gốc.
Sử dụng trong vòng 7 tuần sau khi mở chai thuốc lần đầu.
Đóng gói: Chai 100ml
Thương hiệu: Novartis
Nơi sản xuất: Delpharm Hurningue SAS (Pháp)
Mọi thông tin trên đây chỉ mang tính chất tham khảo. Việc sử dụng thuốc phải tuân theo hướng dẫn của bác sĩ, dược sĩ.
Vui lòng đọc kĩ thông tin chi tiết ở tờ rơi bên trong hộp sản phẩm.




